给出一组实验数据,要求通过对数据的分析,挖掘数据中隐含的化学反应原理和规律,选取适当的数据进行化学计算,这是近年来各种考试中频繁出现的一类试题。虽然这类题目综合性强,难度大,但解答时,还是有规律可寻的,下面举例具体分析说明。
例1. 某学生在课外活动中用一定量的二价金属R和稀硫酸反应来制取氢气,所做5次实验结果的记录如下表(假设每次实验所得的氢气全部被收集,体积在同温同压下测定)。
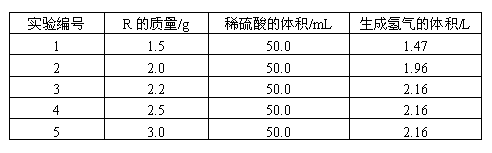
根据上述实验结果进行分析、计算,并回答下列问题:
(1)上述实验中,金属一定过量的组的编号是__________,稀硫酸一定过量的组的编号是__________;
(2)若在当时实验条件下,H2的密度为![]() ,则反应所用金属R的相对原子质量为__________。若所使用的稀硫酸密度为
,则反应所用金属R的相对原子质量为__________。若所使用的稀硫酸密度为![]() ,则反应所用的硫酸溶液中溶质的质量分数为__________。
,则反应所用的硫酸溶液中溶质的质量分数为__________。
解析:(1)实验中所用稀硫酸的体积都相同,在前三组实验中,生成氢气的体积随着金属质量的增加而增加,说明1、2两组实验中稀硫酸一定过量。在4、5两组实验中,再增加金属的质量,生成氢气的体积不再发生改变,说明金属一定过量。在第3组实验中,金属和稀硫酸可能恰好反应,也可能是金属过量。
(2)计算R的摩尔质量应选取稀硫酸过量时的数据计算。设R的摩尔质量为M,取第1(或2)组数据计算,根据![]() 得
得![]() ,解得
,解得![]() ,所以R的相对原子质量为24。
,所以R的相对原子质量为24。
计算稀硫酸的质量分数应取金属过量时的数据计算。取第4(或5)组实验的数据计算,则![]() ,
,![]() ×100%=16.1%。
×100%=16.1%。
例2. 为了测定![]() 混合物的组成,某学生每次称取一定质量的混合物溶于水配成溶液,向其中加入相同浓度的
混合物的组成,某学生每次称取一定质量的混合物溶于水配成溶液,向其中加入相同浓度的![]() 溶液,每次实验均充分反应,实验结果记录如下表:
溶液,每次实验均充分反应,实验结果记录如下表:
|
实验次数 |
混合物的质量/g |
所加Ba(OH)2溶液的体积/L |
测得沉淀的质量/g |
|
1 |
0.858 |
0.5 |
1.379 |
|
2 |
1.716 |
0.5 |
|
|
3 |
2.57 |
0.5 |
4.137 |
|
4 |
3.432 |
0.5 |
5.516 |
|
5 |
4.290 |
0.5 |
5.516 |
|
6 |
5.148 |
0.5 |
5.516 |
请回答下列问题:
(1)第二次实验中产生沉淀的质量是___________________g;
(2)求所用![]() 溶液的物质的量浓度;
溶液的物质的量浓度;
(3)求混合物中![]() 的物质的量之比;
的物质的量之比;
(4)在25℃时,取第3组实验的得溶液体积的1/10,加水配成500mL溶液,求此溶液中![]() 的物质的量浓度(要求写出计算过程)。
的物质的量浓度(要求写出计算过程)。
解析:(1)分析实验数据可以看出,前三次实验中都是![]() 过量,实验2所加样品的质量是实验1的2倍,产生沉淀的质量也应为实验1的2倍,即
过量,实验2所加样品的质量是实验1的2倍,产生沉淀的质量也应为实验1的2倍,即![]() 。
。
(2)以第五组数据计算,此时样品混合物过量,因为![]() ,所以
,所以![]() 。
。
(3)以第一组数据计算,设样品混合物中![]() 的物质的量分别为xmol和ymol,则:
的物质的量分别为xmol和ymol,则:![]() ,即
,即![]() 。
。
(4)设第3次实验中固体混合物中含![]() mol,则含
mol,则含![]() 。
。![]() +
+![]() ,
,![]() 。0.5L
。0.5L![]() 溶液中含
溶液中含![]() 为0.056mol/L×0.5L×2=0.056mol,由
为0.056mol/L×0.5L×2=0.056mol,由![]() ,知
,知![]() 过量
过量![]() ,故
,故![]() 。
。
